Tecnovigilancia es un Sistema de vigilancia postmercado de dispositivos médicos (DM) que identifica, recolecciona, evalúa, gestiona y divulga los eventos o incidentes adversos que presentan los dispositivos médicos (DM) durante su uso, para mejorar la protección de la salud y la seguridad de los pacientes.
La Tecnovigilancia como actividad trascendental dentro del proceso de evaluación y regulación sanitaria y como complemento de un sistema de calidad en salud, requiere de la conformación del programa institucional que le permitan su adecuado desarrollo, es por esto, que tanto los prestadores de servicios de salud y profesionales independientes habilitados, como los fabricantes e importadores de dispositivos médicos de uso en humanos; deben movilizar esfuerzos por generar los elementos necesarios para su buen desarrollo.
Las instituciones deben designar como mínimo, un profesional competente responsable del Programa Institucional de Tecnovigilancia conforme a lo establecido en el numeral 1, articulo 10 de la Resolución 4816 del 27 de noviembre de 2008 “por el cual se reglamenta el Programa Nacional de Tecnovigilancia” y quien deberá dar cumplimiento a los lineamientos mencionados en los artículos 11° y 12°, de la Resolución en cita; por ello es necesario realizar las siguientes inscripciones ante el INVIMA:
- Registro del profesional designado
https://farmacoweb.invima.gov.co/TecnoVigilancia/faces/index.xhtml
- Inscripción a la Red Nacional de Tecno vigilancia.
https://farmacoweb.invima.gov.co/TecnoVigilancia/faces/inscribirRed.xhtml
- REPORTES DE TECNOVIGILANCIA Ingresar
- CONSULTA ALERTAS SANITARIA E INFORME DE SEGURIDAD – REGISTROS SANITARIOS Ingresar
- GESTIÓN RETIROS DEL PRODUCTO DEL MERCADO, INFORMES DE SEGURIDAD, ALERTAS Y HURTOS Ingresar
- CAPACITACIONES Ingresar
- FORMATOS E INSTRUCTIVOS DE INTERES Ingresar
- DOCUMENTOS DE INTERES Ingresar
- NORMATIVIDAD Y COMUNICACIONES Ingresar
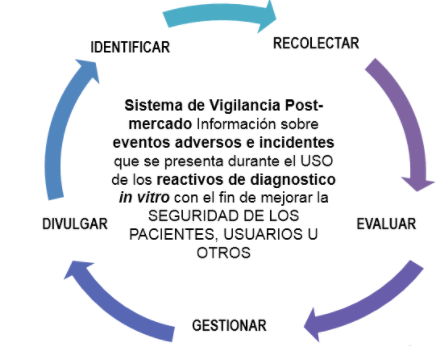
El Programa de Reactivovigilancia, es el conjunto de actividades que tiene por objeto la identificación y cualificación de los efectos indeseados, asociados al uso de los reactivos de diagnóstico in vitro, así como a la identificación de los factores de riesgo o características que puedan estar relacionadas con estos.
El Programa se basa en la notificación, registro y evaluación sistemática de los problemas relacionados con los reactivos de diagnóstico in vitro, con el fin de determinar la frecuencia, gravedad e incidencia de los mismos para prevenir su aparición.
Las actividades que plantea el programa son:
Por lo anterior, las instituciones debe designar como mínimo, un profesional competente responsable del Programa Institucional de reactivovigilancia conforme a lo establecido en el numeral 1, articulo 10 de la Resolución 2020007532 de 2020 “por el cual se modifica el programa nacional de reactivovigilancia” y quien deberá dar cumplimiento a los lineamientos mencionados en los artículos 11° y 12°, de la Resolución en cita; por ello es necesario realizar las siguientes inscripciones ante el INVIMA:
- Registro del profesional designado en plataforma web
- Inscripción a la Red Nacional de Reactivovigilancia.
Asi mismo para el diligenciamiento de los diferentes instrumentos definidos para el sistema de vigilancia de poscomercializacion, se pueden apoyar en el manual de reactivovigilancia web. Manual Reactivovigilancia Web
REPORTES DE REACTIVOVIGILANCIA Ingresar
CONSULTA ALERTAS SANITARIA E INFORME DE SEGURIDAD – REGISTROS SANITARIOS Ingresar
GESTIÓN RETIROS DEL PRODUCTO DEL MERCADO, INFORMES DE SEGURIDAD, ALERTAS Y HURTOS Ingresar
CAPACITACIONES Ingresar
FORMATOS E INSTRUCTIVOS DE INTERES Ingresar
DOCUMENTOS DE INTERES Ingresar
NORMATIVIDAD Y COMUNICACIONES Ingresar
VIGILANCIA SANITARIA PRODUCTOS FARMACEUTICOS
SUSTANCIAS MODELANTES Ingresar